研究内容
細胞内分子輸送機構とその異常に伴う疾病発症機構 (片平)
真核細胞が機能する上で、RNAやタンパク質といった生体分子の細胞内輸送は、きわめて重要です。細胞内輸送機構の破綻は神経疾患やウイルス感染症をはじめとした、さまざまな疾患の原因になることも知られています。本グループでは、RNAの細胞内輸送に焦点を当て、その基本分子機構や疾病との関連について、ゲノム編集、次世代シークエンス解析など、最新の細胞生物学、分子生物学的な手法を取り入れながら研究しています。
- 核―細胞質間における物質輸送
-
内部が高度に区画化された真核細胞では、タンパク質やRNAといった生体分子の細胞内輸送が重要な役割を果たします。最大の細胞内小器官である核は、内部に染色体として遺伝情報を包含し、RNAの転写、プロセシングの場として機能します。一方、タンパク質翻訳装置であるリボソームは細胞質に存在します。このように遺伝子発現の各過程が、細胞内の異なるコンパートメントで行なわれるため、RNAの転写に必要なRNAポリメラーゼや転写因子のようなタンパク質は、細胞質で翻訳された後に核内へ、逆に、核内で転写されたRNAは、タンパク質翻訳過程で機能するために細胞質へ、それぞれ輸送される必要があります。つまり、真核生物の遺伝子発現には、核-細胞質間における両方向性の輸送が関係するわけです。
核は周囲を核膜という脂質膜で覆われています。そのため、RNAやタンパク質といった水溶性の物質は核と細胞質の間を自由に行き来することができません。核膜孔複合体(nuclear pore complex: NPC)は核膜に開口したチャネルで、RNAやタンパク質はこのチャネルを通って核と細胞質の間を往来します。RNAやタンパク質のNPC通過をサポートするのが、”輸送受容体“と総称されるNPCと相互作用する性質を持ったタンパク質因子群です。インポーチン-bファミリータンパク質群は、輸送受容体のうち最も種類が多く、さまざまなタンパク質やマイクロRNA、tRNA(transfer RNA)、核内低分子RNA(snRNA)といった比較的低分子量のRNAの輸送に関わります。一方、タンパク質翻訳の鋳型となるmRNAの輸送は、Tap-p15(NXF1-NXT1)というインポーチン-bファミリーに属さない特有の輸送受容体が担います。私たちのグループの研究のルーツは、20年ほど前のmRNA輸送受容体の同定に遡ります。
- 輸送受容体による積み荷選択
-
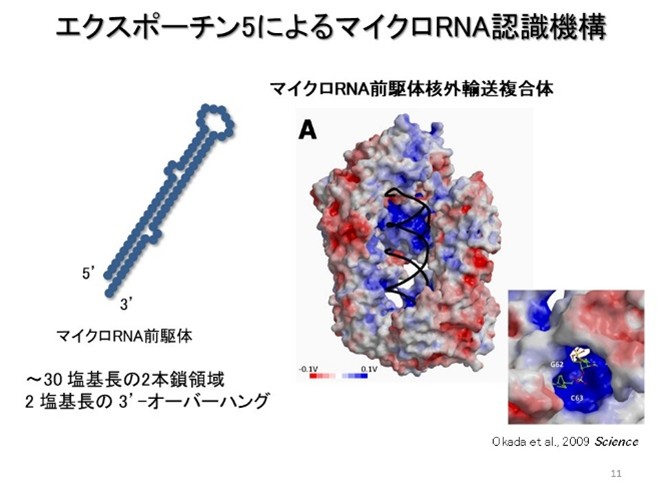
真核細胞内には、マイクロRNA、tRNA、snRNA、mRNAなど、さまざまなRNAが存在します。輸送受容体は、細胞内に数多存在するRNAの中から、それぞれが輸送すべき”積み荷“として、特定のRNAを選び出し結合します。インポーチン-bファミリータンパク質の場合、それぞれの輸送受容体は、積み荷となるRNAの構造上の特徴を”輸送シグナル“として識別し、特異的に結合します。例えば、マイクロRNA輸送受容体であるエクスポーチン-5は、マイクロRNA前駆体の2本鎖領域と3’末端のオーバーハングを認識します。Tap-p15はRNA結合タンパク質ですが、RNAの特定の塩基配列や構造を識別することができません。例えば、試験管内の結合実験では、本来の積み荷ではないtRNAにも結合します。このような問題は、Tap-p15が、転写やプロセシングの際にmRNAに結合するmRNA結合タンパク質を”アダプター“とし、間接的にmRNAを積み荷として認識することにより解決されます。
- mRNAプロセシングと核外輸送との共役
-
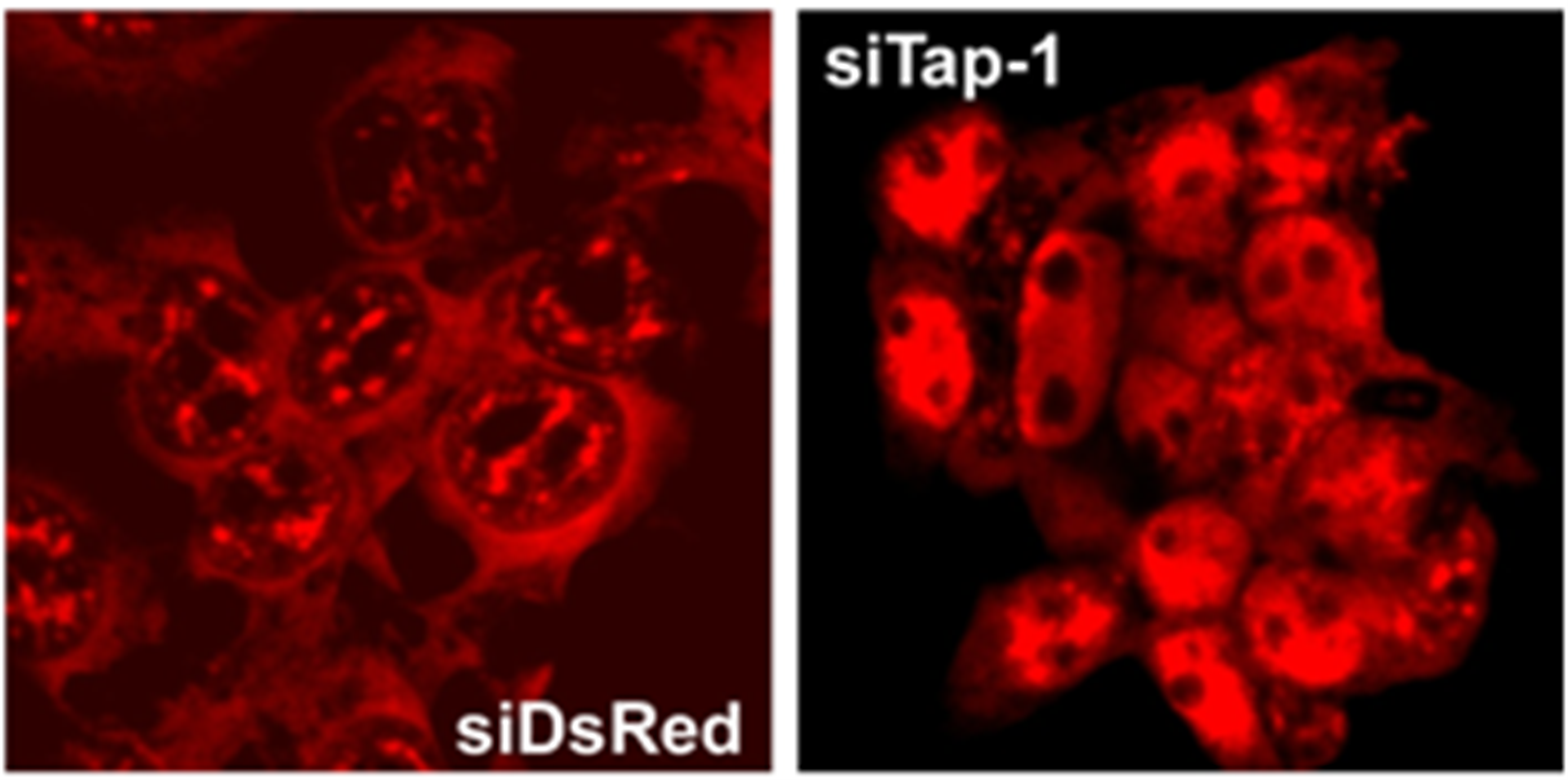
mRNAは転写された後、キャップ付加、スプライシング、ポリアデニル化といった転写後のプロセシングを経て成熟した後、細胞質へ輸送されタンパク質翻訳の鋳型として機能します。その間、mRNAは”裸“の状態でいることはなく、さまざまなタンパク質と会合し、mRNP(mRNA-タンパク質複合体)として存在します。mRNA結合タンパク質の中には、Tap-p15と選択的に結合するタンパク質が存在します。TREX(TRanscription-EXport)複合体は、RNAポリメラーゼII(RNAPII)によるmRNAの転写/プロセシングと核外輸送を共役させる上で重要な役割を果たすタンパク質複合体です。このタンパク質複合体は、mRNAの転写に関わるRNAPIIと相互作用し、染色体上で活発に転写されている領域に集まってきます。TREX複合体のコンポーネントの一つであるALYREFというmRNA結合タンパク質は、転写/プロセシングの過程でmRNAに結合すると輸送受容体であるTap-p15に結合し、輸送受容体と積み荷であるmRNAを結びつけるアダプターとして機能します。また、同じくTREX複合体のTHOC5というコンポーネントが、ALYREFとともにコアダプターとして機能することも見出しました。
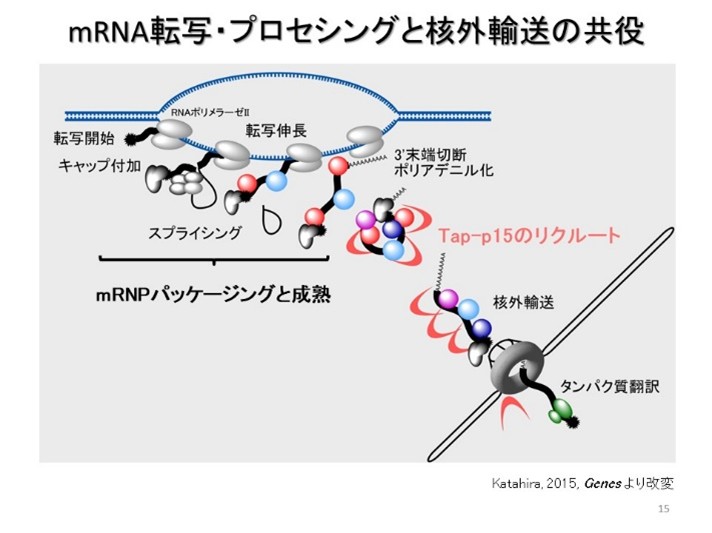
TREX複合体はRNAPIIやmRNA輸送受容体Tap-p15ばかりでなく、転写伸長因子、mRNA前駆体のスプライシングやポリアデニル化、転写終結に関係するタンパク質因子とも相互作用します。ポリアデニル化因子や転写終結因子との相互作用を介して、TREX複合体が、ポリアデニレーション部位の選択の過程やプロセシングの完了に伴うmRNAの遺伝子からの解離の過程に関係していることも明らかにしています。 - 核-細胞質間輸送と疾病
-
核-細胞質間輸送は真核細胞における遺伝子発現に必須のプロセスであり、輸送の阻害は細胞、ないしは、個体の死につながります。また、完全な輸送阻害が起こらなくても、例えば、TREX複合体の機能不全に伴い、輸送されなかったmRNAがゲノム上の転写部位近傍に蓄積し、DNA複製阻害やDNA切断が起こることにより、ゲノムが不安定化することも知られています。TREX複合体のコンポーネントのヒトゲノム上における分布をChIP-seqという手法を用いて調べ、ゲノムの中でも特に不安定な領域として知られている反復配列を含んだ領域に集積していること、TREX複合体の機能阻害により、DNAに二重鎖切断が起こることを明らかにしています。
mRNAの核外輸送は真核生物の遺伝子発現に必須であるばかりでなく、核内で生活環の一部を営むウイルスのような病原体の増殖・複製にも必要です。また、ある種のウイルスは、自身の増殖・複製に有利な環境を作るために、mRNA輸送過程を阻害し、宿主の抗ウイルス遺伝子発現に対抗することも知られています。このようなことから、mRNAの輸送過程は、抗感染症創薬のターゲットにもなり得ます。現在、研究室では、ウイルス因子によるmRNA核外輸送阻害機構や輸送阻害による疾病発症機構に関する研究も行なっています。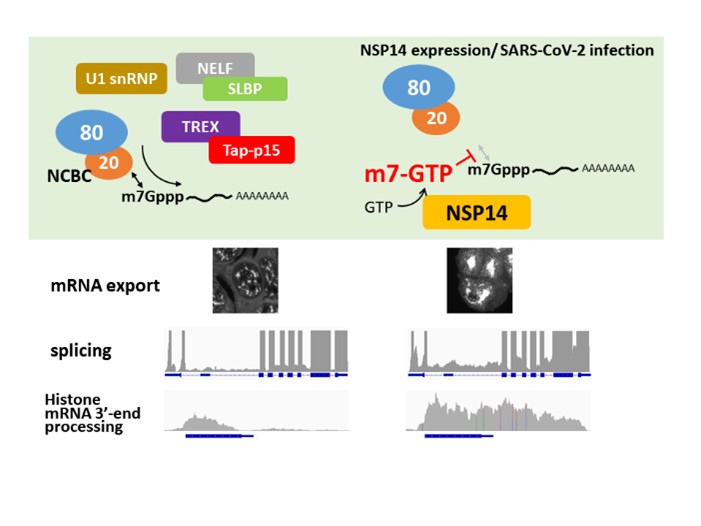
変性分子を標的とした加齢性・炎症性疾患の病態解明と制御 (板倉)
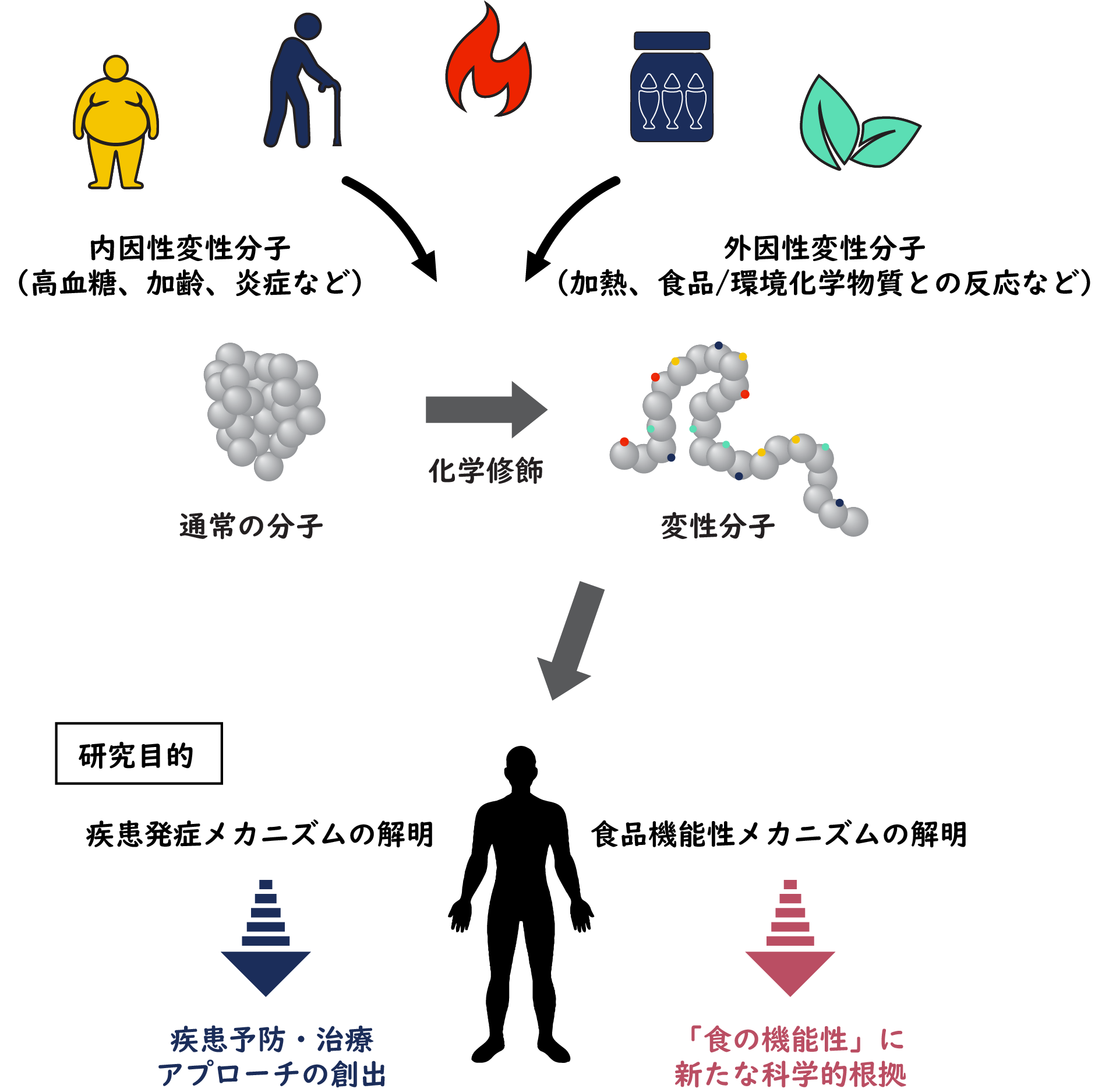
「細胞は周囲環境をどのように感知するのか、その制御は可能か」という関心に基づき、変性分子(酸化、糖化、凝集タンパク質など) による炎症応答や細胞死誘導について研究を進めています。
もう少し具体的には、タンパク質などの生体分子は、加齢や炎症などの内的要因、および食品成分や環境化学物質との反応などの外的要因により、本来の機能を失った変性分子に変換されます。
このような変性分子は、新たな機能性を持つことがありますが、一般的には生体にとってのただのゴミのように理解されることが多く、あまり研究が進められておりません。
変性分子による細胞・生体応答について研究を展開することで、将来的に、疾患予防・治療アプローチを創り出すことや、科学的根拠が乏しい食の機能性に新たな根拠を加えたいと考えています。
分子レベルから個体レベルに至るまで、多岐にわたる実験手法を駆使し、加齢性疾患や炎症性疾患(アルツハイマー病、脳卒中など)の病態形成メカニズムを明らかにし、その制御法を確立することで、新たな治療法、予防法の開発を目指します。