がん免疫療法のためのナノワクチンシステム
免疫とは、ウイルスや細菌などの感染から身体を守る仕組みのことです。がん免疫療法は、このような生体防御機構である免疫を、がん治療に展開するものです。がん免疫療法が確立できれば、安全性の高い究極の個人対応型(パーソナライズド)治療になると期待されています。
免疫応答には、自然免疫と獲得免疫があります。自然免疫では、マクロファージや好中球などの貪食細胞が中心となり、侵入してきた病原体などの異物を食べて排除します。獲得免疫では、外部から侵入してきた病原体を特異的に認識するプロセスを経て、異物の情報(抗原)によって教育を受けた異物特異的なB細胞やT細胞が防御・排除を担います。獲得免疫には、免疫細胞(細胞傷害性T細胞)が、ウイルス感染細胞などを直接攻撃する細胞性免疫と、抗体で異物を不活化する液性免疫があります。がん免疫療法では、がん細胞などの異常細胞を特異的に認識する獲得免疫を誘導して、治療を行います。
標的特異的な免疫誘導は、樹状細胞を中心とする抗原提示細胞が、異常細胞を識別するための目印(抗原)を免疫担当細胞に提示することで起こります。抗原提示細胞による抗原の提示には、MHCクラスⅠもしくはクラスⅡの2種類の分子による経路があります。抗原が、貪食によって抗原提示細胞に取り込まれた場合、細胞内のエンドソーム/リソソームにおいて処理されてペプチド断片となり、細胞上のMHCクラスⅡ分子に乗せられて提示されます。MHCクラスⅡ分子上に提示された抗原はヘルパーT細胞に認識され、液性免疫の誘導につながります。 一方、抗原が抗原提示細胞のサイトゾル中に存在する場合、プロテアソームによる処理を受けてペプチド断片となり、細胞上のMHCクラスⅠ分子に乗せられて提示されます。MHCクラスⅠ分子上に提示された抗原は、細胞傷害性T細胞を活性化させ、細胞性免疫の誘導につながります。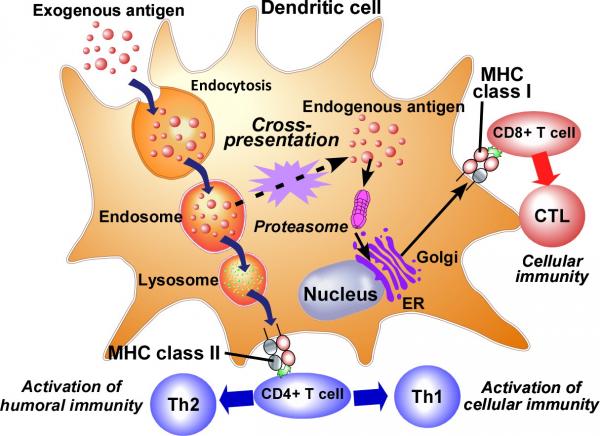
がん免疫療法において、がん細胞などの異常細胞の排除には、細胞性免疫が重要な役割を果たしています。したがって、がん免疫療法の実現には、外来性抗原を抗原提示細胞のサイトゾルに運搬して、MHCクラスⅠ経路の抗原提示により細胞性免疫を誘導する抗原デリバリーシステムの開発が必要不可欠です。私たちは、機能性リポソームを中心に、細胞内の適切な場所に抗原を送り届けて、効果的に免疫を誘導するナノワクチンシステムについて研究を進めています。 また、リポソームにがん免疫を活性化する様々な機能性分子を組み込むことで、その高性能化を図っています。
本テーマに関する主な論文
- E. Yuba, R. K. Gupta, Preparation of glycopeptide-modified pH-sensitive liposomes for promoting antigen cross-presentation and induction of antigen-specific cellular immunity, Biomater. Sci., 12, 1490-1501 (2024).
- E. Yuba, Y. Kado, N. Kasho, A. Harada, Cationic lipid potentiated the adjuvanticity of polysaccharide derivative-modified liposome vaccines, J. Control. Release, 362, 767-776 (2023).
- S. Yanagihara, N. Kasho, K. Sasaki, N. Shironaka, Y. Kitayama, E. Yuba, A. Harada, "pH-Sensitive branched β-glucan-modified liposomes for activation of antigen presenting cells and induction of antitumor immunity", J. Mater. Chem. B, 9, 7713-7724 (2021). DOI: 10.1039/d1tb00786f
- E. Yuba, Y. Sugahara, Y. Yoshizaki, T. Shimizu, M. Kasai, K. Udaka, K. Kono, “Carboxylated polyamidoamine dendron-bearing lipid-based assemblies for precise control of intracellular fate of cargo and induction of antigen-specific immune responses”, Biomaterials Science, 9, 3076-3089 (2021). DOI:10.1039/D0BM01813A
- E. Yuba, A. Yamaguchi, Y. Yoshizaki, A. Harada, K. Kono, “Bioactive polysaccharide-based pH-sensitive polymers for cytoplasmic delivery of antigen and activation of antigen-specific immunity”, Biomaterials, 120, 32-45 (2017). DOI: 10.1016/j.biomaterials.2016.12.021.
- E. Yuba, N. Tajima, Y. Yoshizaki, A. Harada, H. Hayashi, K. Kono, "Dextran derivative-based pH-sensitive liposomes for cancer immunotherapy", Biomaterials, 35, 3091-3101 (2014). DOI:10.1016/j.biomaterials.2013.12.024
- E. Yuba, A. Harada, Y. Sakanishi, S. Watarai, K. Kono, "A liposome-based antigen delivery system using pH-sensitive fusogenic polymers for cancer immunotherapy", Biomaterials, 34, 3042-3052 (2013).