当科で行っている研究
当科では多くの臨床研究、基礎研究を行っていますが、代表的なものを紹介します。
臨床研究
移植後シクロホスファミド(posttransplantation cyclophosphamide: PTCy)によるGVHD予防法の我が国における臨床導入、および至適化に向けた研究
HLA半合致移植について
同種造血幹細胞移植は現在でも難治性血液悪性疾患を完治に導きうる有効な治療法です。HLA*適合血縁ドナーが同種造血幹細胞移植のドナーの第一選択となりますが、血縁者間に適切なドナーがいない場合には骨髄バンクでHLA適合非血縁ドナーをコーディネートすることになります。しかしながら病勢により至適な時期に移植を受けられないケースが少なからずあります。
HLA半合致ドナーとは2つのHLAハプロタイプのうち1つが合致しているドナーであり、親子では100%で半合致しており、同胞でも50%の確率で半合致しているため、患者さんの90%以上でドナーが見つかることになります。しかしながらHLA半合致移植(ハプロ移植)はHLAの不一致により重症の移植片対宿主病(GVHD)*や移植片の拒絶が生じる可能性があり、これまではGVHDの原因となるT細胞除去などの高価で複雑な操作や強力な免疫抑制療法を必要としてきました。一方で強力な免疫抑制療法やT細胞の除去は再発率を上昇させることになり、歴史的にさまざまなハプロ移植が試みられていましたが、一種のジレンマに陥っていました。
*HLA( Human leukocyte antigen):ヒト白血球抗原
*GVHD:graft-verus-host disease
PTCyハプロ移植について
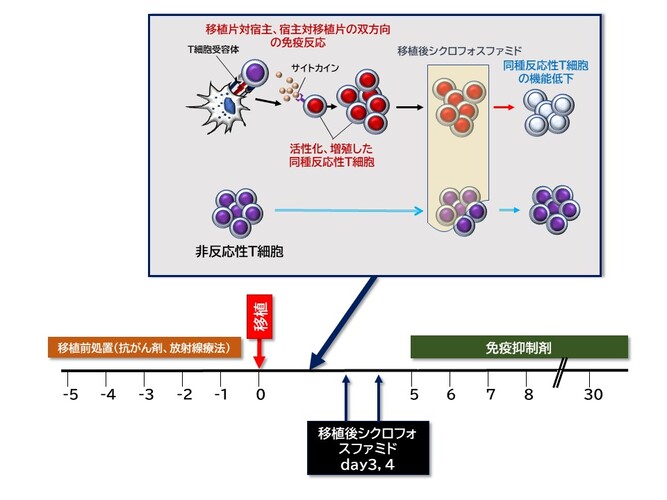
移植後シクロホスファミド(posttransplantation cyclophosphamide: PTCy)を用いたGVHD予防法 によるハプロ移植(PTCyハプロ)は、2002年に米国のJohns Hopkins Groupにより世界初の臨床研究が報告されました¹。 当初は移植後にシクロホスファミドを投与することによってGVHDや拒絶などの原因となる同種反応を示す有害なT細胞を選択的に除去すると考えられていましたが、最近の研究で 同種反応を示すT細胞は残存しており、その機能を低下させることが分かってきました²(図)。現在、PTCyの安全性、及び簡便性から国際的に広がりを見せており、同種造血幹細胞移植におけるドナープールの拡大に大きく寄与しています。
(参考文献)
1. Biol Blood Marrow Transplant. 2002;8(7):377-86.
2. J Clin Invest. 2019;129(6):2357-2373.
当教室で行っているハプロ移植研究について
我々は我が国で初めて臨床研究として2010年1月にPTCyハプロを行いました1)。その後2025年3月までに202例のPTCyハプロを行ってきました。そして、これまでの臨床研究において、移植片に含まれる造血幹細胞数が移植後の予後に大きな影響を与えることを解明しました2)。また、KIR2DS1陽性ドナーからのPTCyハプロが移植時寛解例において再発の抑制に有意に寄与していることを報告しました3)。さらにNKG2D一塩基多型である、rs1049174 CCドナーからのPTCyハプロが再発/進行のリスク低下と関連していることを実証しました4)。また、HLA適合血縁者・非血縁者間においてもPTCyによるGVHD予防が有用であることを我が国で初めての前向き研究として報告しました5)。 その後もPTCyを用いた移植に関する研究を多数行い、発表してきました(当科PTCy関連業績)。
現在、PTCyハプロにおける最適なドナーに関する特定臨床研究「造血器悪性腫瘍に対する最適ドナーを考慮した移植後シクロフォスファミドを用いた血縁HLA半合致移植」を行っています(jRCTs051190011)。さらに PTCyをHLA不適合非血縁間移植への拡大を目的とした「HLAミスマッチ骨髄バンクドナーからの同種造血細胞移植における移植後シクロホスファミドを用いた GVHD予防法の安全性と有効性に関する臨床第 II相試験」の特定臨床研究(jRCTs051220057)も施行中です。今後PTCyハプロにおける至適条件の確立に向けて精力的に研究を行っていく予定です。
(当科PTCy関連業績)
-
Nakamae H, et al. HLA Haplo-Identical Peripheral Blood Stem Cell Transplantation Using High-Dose Cyclophosphamide Post-Transplantation For Poor Prognosis Or Refractory Acute Leukemia and Myelodysplastic Syndrome: A Prospective Pilot Study At a Single Center. Blood (2013) 122 (21): 3404.
- Nakamae H, et al. HLA haploidentical peripheral blood stem cell transplantation using reduced dose of posttransplantation cyclophosphamide for poor-prognosis or refractory leukemia and myelodysplastic syndrome. Exp Hematol. 2015 Nov;43(11):921-929.e1. doi: 10.1016/j.exphem.2015.07.006. Epub 2015 Aug 15. PMID: 26284307
- Nakamae H, et al. A Prospective Study of an HLA-Haploidentical Peripheral Blood Stem Cell Transplantation Regimen Based on Modification of the Dose of Posttransplant Cyclophosphamide for Poor Prognosis or Refractory Hematological Malignancies. Cell Transplant. 2022 Jan-Dec;31:9636897221112098. doi: 10.1177/09636897221112098. PMID: 35906755
-
Nishimoto M, et al. Clinical Impacts of Using Serum IL-6 Level as an Indicator of Cytokine Release Syndrome after HLA-Haploidentical Transplantation with Post-Transplantation Cyclophosphamide. Biol Blood Marrow Transplant. 2019 Oct;25(10):2061-2069. doi: 10.1016/j.bbmt.2019.06.003. Epub 2019 Jun 10. PMID: 31195139
- Ido K, et al. Donor KIR2DS1-Mediated Decreased Relapse and Improved Survival Depending on Remission Status at HLA-Haploidentical Transplantation with Post-Transplantation Cyclophosphamide. Biol Blood Marrow Transplant. 2020 Apr;26(4):723-733. doi: 10.1016/j.bbmt.2019.12.765. Epub 2019 Dec 31. PMID: 31899360
- Ido K, et al. Effect of Donor NKG2D Polymorphism on Relapse after Haploidentical Transplantation with Post-Transplantation Cyclophosphamide. Transplant Cell Ther. 2022 Jan;28(1):20.e1-20.e10. doi: 10.1016/j.jtct.2021.09.019. Epub 2021 Oct 1. PMID: 34607074
- Nakamae H, et al. A phase II study of post-transplant cyclophosphamide combined with tacrolimus for GVHD prophylaxis after HLA-matched related/unrelated allogeneic hematopoietic stem cell transplantation. Int J Hematol. 2022 Jan;115(1):77-86. doi: 10.1007/s12185-021-03228-1. Epub 2021 Sep 29. PMID: 34586587
-
Nakamae H. Systematic overview of HLA-matched allogeneic hematopoietic cell transplantation with post-transplantation cyclophosphamide. Int J Hematol. 2022 Oct;116(4):465-481. doi: 10.1007/s12185-022-03428-3. Epub 2022 Aug 5. PMID: 35930118
-
Makuuchi Y, et al. Posttransplant cyclophosphamide contributes to the impairment of the graft-versus-leukemia effect and the amelioration of graft-versus-host disease with the suppression of alloreactive T cells in a murine stem cell transplant model. Exp Hematol. 2023 Jul;123:56-65. doi: 10.1016/j.exphem.2023.04.003. Epub 2023 Apr 23. PMID: 37098360
-
Nakaya Y, et al.Effect of graft cell dose on second transplantation from a haploidentical donor with post-transplantation cyclophosphamide for relapsed/refractory acute leukemia. Bone Marrow Transplant. 2023 Aug;58(8):947-949. doi: 10.1038/s41409-023-01986-6. Epub 2023 Apr 28. PMID: 37117265
-
Harada N, et al. Third HLA-haploidentical stem cell transplantation using post-transplant cyclophosphamide for relapsed acute leukemia. Bone Marrow Transplant. 2023 Dec;58(12):1403-1405. doi: 10.1038/s41409-023-02108-y. Epub 2023 Sep 15. PMID: 37714944
- Nakaya Y, et al.HLA-Haploidentical Peripheral Blood Stem Cell Transplantation with Post-Transplantation Cyclophosphamide versus HLA-Matched Unrelated Donor Transplantation for Myelodysplastic Syndrome. Transplant Cell Ther. 2024 Mar;30(3):316.e1-316.e12. doi: 10.1016/j.jtct.2023.10.021. Epub 2023 Oct 30. PMID: 3810826
-
Hirose A, et al. A comparison of long-term outcomes by donor type in the era of post-transplantation cyclophosphamide for aggressive adult T-cell leukemia/lymphoma. Bone Marrow Transplant. 2024 May;59(5):695-698. doi: 10.1038/s41409-024-02231-4. Epub 2024 Feb 14. PMID: 38355910
-
Nakaya Y, et al. Peripheral blood stem cell transplantation using HLA-haploidentical donor with post-transplant cyclophosphamide versus HLA-matched sibling donor for lymphoma. Bone Marrow Transplant. 2024 May;59(5):630-636. doi: 10.1038/s41409-024-02229-y. Epub 2024 Feb 14. PMID: 38355911
-
Moriguchi M, et al.Impacts of Posttransplant Cyclophosphamide Dose on Graft-versus-Leukemia Effects via HLA-B Leader in HLA-Haploidentical Peripheral Blood Stem Cell Transplantation. Acta Haematol. 2024;147(6):661-670. doi: 10.1159/000538078. Epub 2024 Mar 1. PMID: 38432202
-
Nakamae H. Graft-versus-tumor effect of post-transplant cyclophosphamide-based allogeneic hematopoietic cell transplantation. Front Immunol. 2024 Jun 6;15:1403936. doi: 10.3389/fimmu.2024.1403936. eCollection 2024. PMID: 38903503
-
Ido K, et al. Effect of peptide-binding motif on survival of HLA-haploidentical transplantation with post-transplant cyclophosphamide. Br J Haematol. 2024 Sep;205(3):1077-1096. doi: 10.1111/bjh.19630. Epub 2024 Jul 7. PMID: 38972374
-
Hayashi T, et al.Posttransplantation cyclophosphamide mediates effective reconstitution of memory B cells after allogeneic hematopoietic cell transplantation. Eur J Haematol. 2024 Nov;113(5):651-663. doi: 10.1111/ejh.14280. Epub 2024 Jul 28. PMID: 39072897
-
Fuji S, Nakamae H, et al. Lower-dose post-transplant cyclophosphamide in haploidentical hematopoietic cell transplantation. Bone Marrow Transplant. 2024 Nov;59(11):1628-1630. doi: 10.1038/s41409-024-02405-0. Epub 2024 Aug 26. PMID: 39187600
-
Moriguchi M, et al. Comparison of HLA-haploidentical donors with post-transplant cyclophosphamide versus HLA-matched unrelated donors in peripheral blood stem cell transplantation for acute myeloid leukaemia. Br J Haematol. 2024 Dec;205(6):2376-2386. doi: 10.1111/bjh.19825. Epub 2024 Oct 22. PMID: 39439234
-
Nakaya Y, et al. Dose Effect of Antithymocyte Globulin or Post-transplant Cyclophosphamide in Haploidentical Peripheral Blood Stem Cell Transplantation: A Comparative Study. Transplant Cell Ther. 2025 Apr 26:S2666-6367(25)01142-X. doi: 10.1016/j.jtct.2025.04.007. Online ahead of print. PMID: 40294821
同種造血細胞移植後の再発機序に関する研究
「ベネトクラックスによって誘導されたBCL-2発現の高いT細胞は、抗白血病免疫の「移植対白血病効果」に影響を与える。」
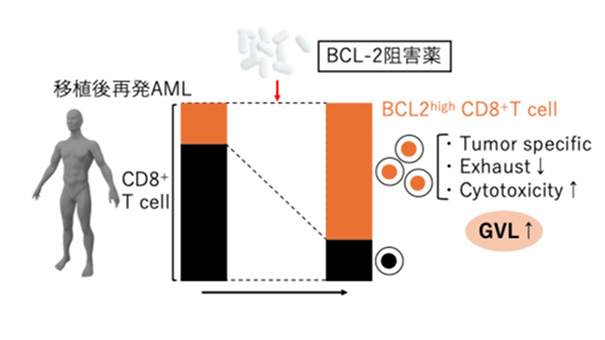
同種造血幹細胞移植 (allo-HCT) は血液腫瘍に有効な治療ですが、早期再発も多く長期奏功の本態解明が急がれます。我々は不明点が多いAllo-HCT後の移植片対白血病(GVL)効果に着目してBCL-2阻害薬が奏功したallo-HCT後再発白血病患者の免疫細胞を解析し、ドナー由来BCL-2高発現CD8陽性T細胞が腫瘍特異的で強い細胞傷害活性を有し、GVL効果の中心を担っている可能性を示しました(以下、文献)。さらにこれらのBCL-2高発現T細胞は長期GVL効果の維持に関与すると考えられたため、現在それらの検証を行なっています。本研究はGVL効果の本体解明、新規バイオマーカー開発や次世代細胞療法への応用が期待されます。
(文献)
Nagasaki J, et al. T cells with high BCL-2 expression induced by venetoclax impact anti-leukemic immunity "graft-versus-leukemia effects". Blood Cancer J. 2024 May 14;14(1):79. doi: 10.1038/s41408-024-01064-0. PMID: 38744860
同種造血細胞移植後の補体関連研究
「移植関連血栓性微小血管症(TA-TMA)の早期予測マーカーとしての補体因子Baの有用性」
同種造血幹細胞移植(allo-HSCT)後に発症する重篤な合併症である移植関連血栓性微小血管症(TA-TMA)における補体活性化の関与を解明し、その予測バイオマーカーとしての補体因子Baの有用性を明らかにしたものです。当科での30症例(TA-TMA 15例、非TA-TMA 15例)を対象としたnested case-control研究において、17種類の補体関連遺伝子の稀な変異頻度には両群で有意差がみられませんでした。一方で、移植7日目の血漿中Ba濃度はTA-TMA群で有意に高値を示し、その後のTA-TMA発症および非再発死亡(NRM)と有意な関連を認めました。ROC解析ではBa値869.1 ng/mlをカットオフとし、感度80%、特異度100%、陽性的中率100%と極めて高い予測精度を示した。また、Ba高値群では急性GVHDの発症も多く、補体活性化が内皮障害とGVHDを介してTA-TMAの発症に関与している可能性が示唆されました。
本研究は、Ba濃度を用いた早期スクリーニングと予防的介入の有効性を示すとともに、新たな補体阻害療法の開発と適応選別に資する重要な知見を提供しています。
(文献)
Okamura H, et al. Early Elevation of Complement Factor Ba Is a Predictive Biomarker for Transplant-Associated Thrombotic Microangiopathy. Front Immunol. 2021 Jul 13;12:695037. doi: 10.3389/fimmu.2021.695037. eCollection 2021. PMID: 34326846
機械学習を活用した造血幹細胞移植後予後予測に関する研究
「機械学習を活用した造血幹細胞移植後予後予測アプリの開発と応用」
本研究は、同種造血幹細胞移植(allo-HCT)を受けた患者の個別予後を、客観的かつ視覚的に提示するインタラクティブなウェブアプリケーションの開発を目的としました。
予後予測には、ランダムサバイバルフォレスト(Random Survival Forest: RSF)という機械学習モデルを採用し、年齢、疾患リスク、併存疾患スコア、ドナーの種類や性別不一致など、移植前に把握可能な8つの臨床因子を入力することで、1年後の全生存率(OS)、無増悪生存率(PFS)、再発率、非再発死亡率(NRM)をそれぞれ予測できます。
このモデルは、大阪市立大学で2011年から2020年にかけて施行された363例の移植データを用いて訓練・検証され、AUC(C-index)は0.70〜0.77と高い予測性能を示しました。従来の単純なリスク分類では捉えきれない個々の背景を加味した個別予測が可能であり、より現実的な臨床判断への応用が期待されます。
また、開発されたアプリはWeb上で一般公開されており、医療従事者が容易にアクセスし、治療方針の説明や患者へのインフォームドコンセント支援として活用できます(https://predicted-os-after-transplantation.shinyapps.io/RSF_model/)。
今後は、他施設データでの外部検証や、施設独自のモデルへのカスタマイズなど、さらなる実用化に向けた展開が期待されています。
(文献)
Okamura H, et al. Interactive Web Application for Plotting Personalized Prognosis Prediction Curves in Allogeneic Hematopoietic Cell Transplantation Using Machine Learning. Transplantation. 2021 May 1;105(5):1090-1096. doi: 10.1097/TP.0000000000003357. PMID: 32541556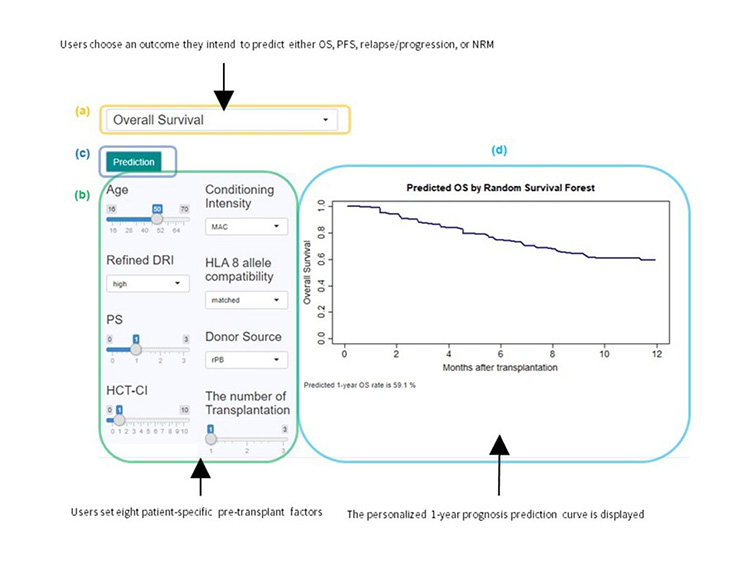 基礎研究
基礎研究
基礎研究
血液腫瘍動物モデルを用いた研究
<ロペグインターフェロンの抗腫瘍メカニズムの解明>
ロペグインターフェロンは、体内での消失半減期が長く、頻回の投与を必要としない新規のインターフェロン-α製剤です。近年、血液がんの一種である骨髄増殖性腫瘍を分子学的寛解へ導く可能性があることが示されています。
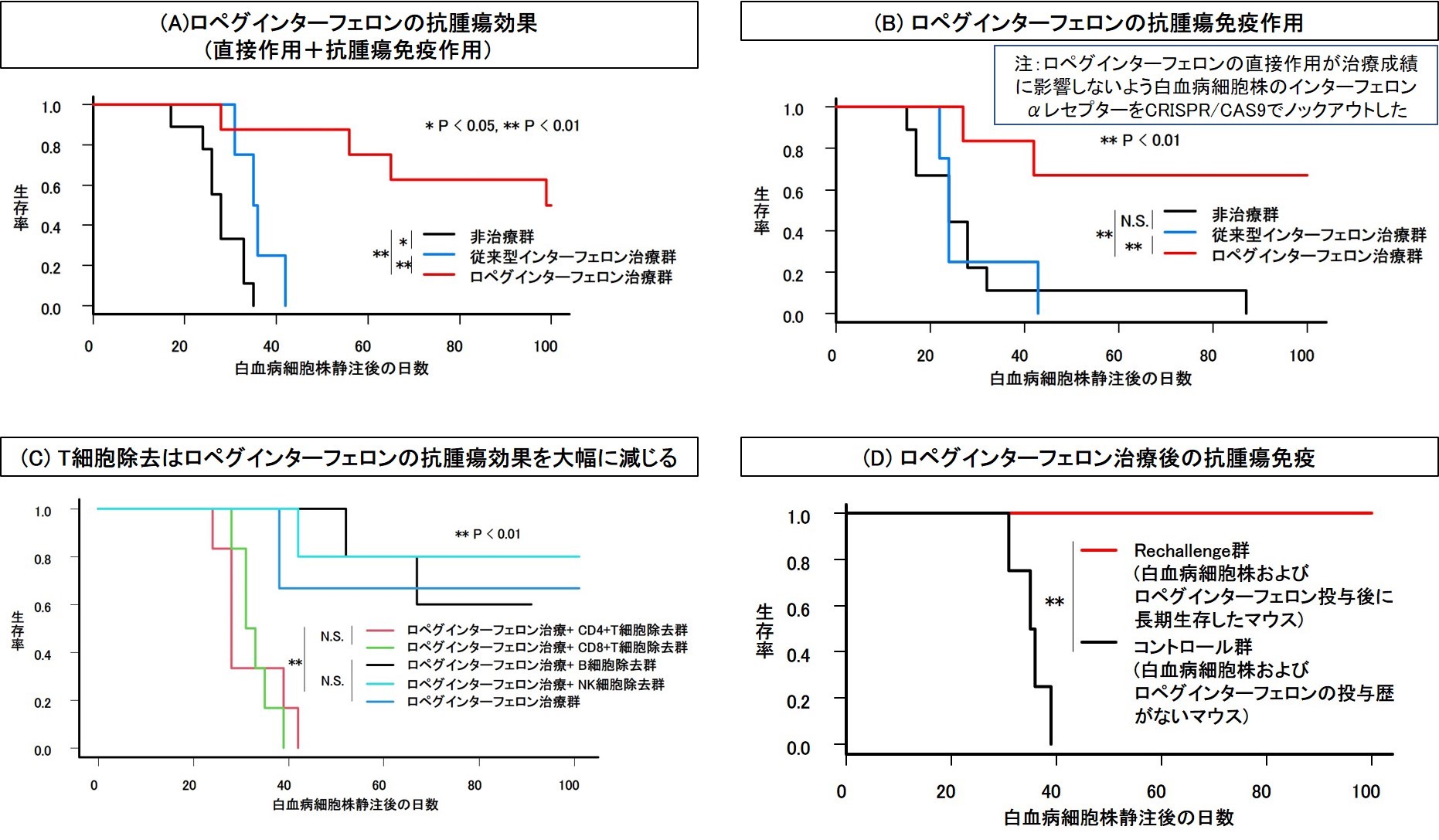
インターフェロン-αのがん抑制における機能のメカニズムは、①腫瘍細胞にアポトーシスや細胞分裂の停止を誘導する直接効果、②宿主の免疫細胞を活性化することにより腫瘍を体内から排除する免疫調整作用に大別されます。しかし生体内においていいずれが重要なのか、従来のインターフェロンαならびにロペグインターフェロンとも明らかでありませんでした。我々はインファーフェロンαの抗腫瘍作用機序について直接作用および免疫調整作用の両側面から検討しました(Cancer Sci. 2022;113:2246-2257)。免疫抑制処置を行う必要なくC57BL/6(B6)マウスに生着する白血病細胞株を用いて独自の白血病マウスモデルを作成し、①ロペグインターフェロンは従来のインファーフェロンαより白血病マウスの生存期間を有意に延長すること (下図A)、②抗腫瘍免疫作用がロペグインターフェロンの主要な抗腫瘍機序であること(下図B)、③T細胞がロペグインターフェロン治療において重要な働きを担うこと(下図C)、ロペグインターフェロンにより腫瘍が排除された生体内で記憶免疫が誘導されること(図D)を明かにしました。
(文献)
Sakatoku K, et al. Immunomodulatory and direct activities of ropeginterferon alfa-2b on cancer cells in mouse models of leukemia. Cancer Sci. 2022 Jul;113(7):2246-2257. doi: 10.1111/cas.15376. Epub 2022 May 2.PMID: 35441749