審査申請
申請から研究開始までの手続き
標準業務手順書
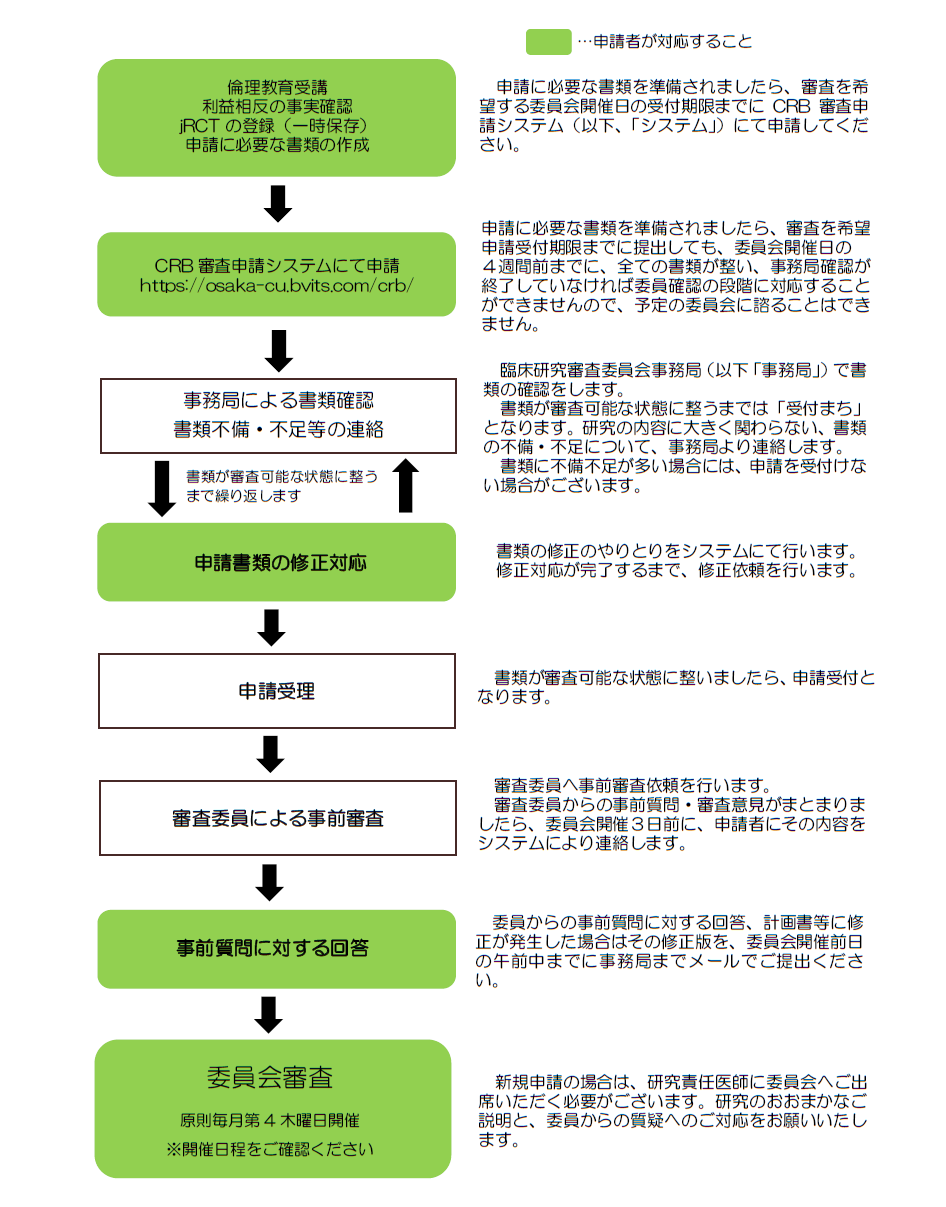
・臨床研究法に基づく臨床研究の実施に関わる標準業務手順書(20231201制定 2.0版)申請から審査までのフロー
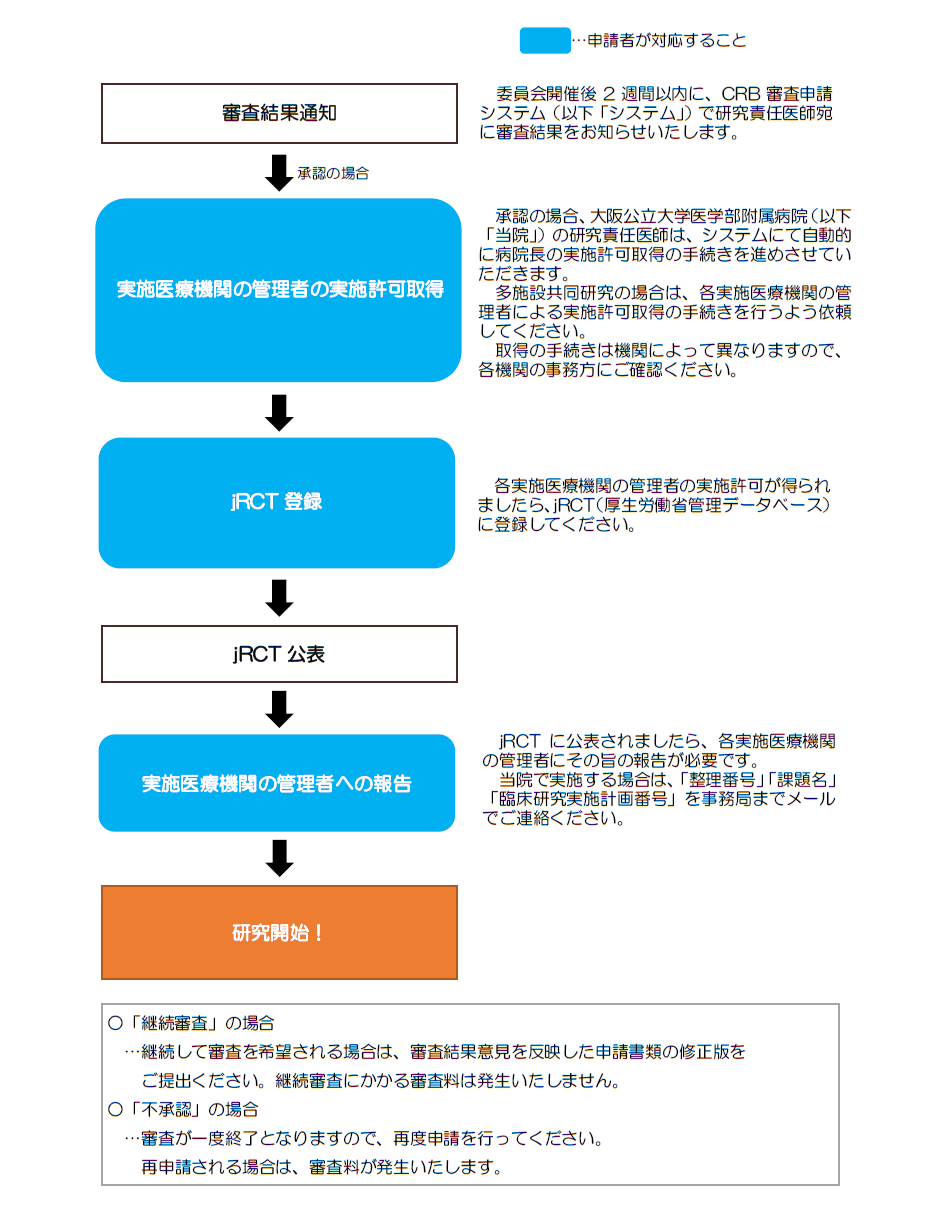
承認後から研究開始までのフロー

必要な書類
・書類をダウンロードするには、各申請項目をクリックしてください。該当欄へジャンプできます。
・使用する書式についての説明は厚生労働省「臨床研究法の統一書式について」をご覧ください。
特定臨床研究 ・ 非特定臨床研究
単施設・当院が代表の多施設共同研究
当院が分担施設として参加する多施設共同研究
申請別書類一覧
臨床研究法遵守で実施する特定臨床研究・非特定臨床研究(努力義務)
|
臨床研究法遵守の研究のうち、当院が分担施設として参加(研究実施許可取得)
|
モニタリング・監査について
本学で実施中の研究に係るモニタリング及び監査の手続き等につきましては、倫理委員会事務局(★を@に変更してください)までお問い合わせください。
臨床研究法における利益相反管理
利益相反管理フロー( 単施設研究の場合 ・ 多施設共同研究の場合 )
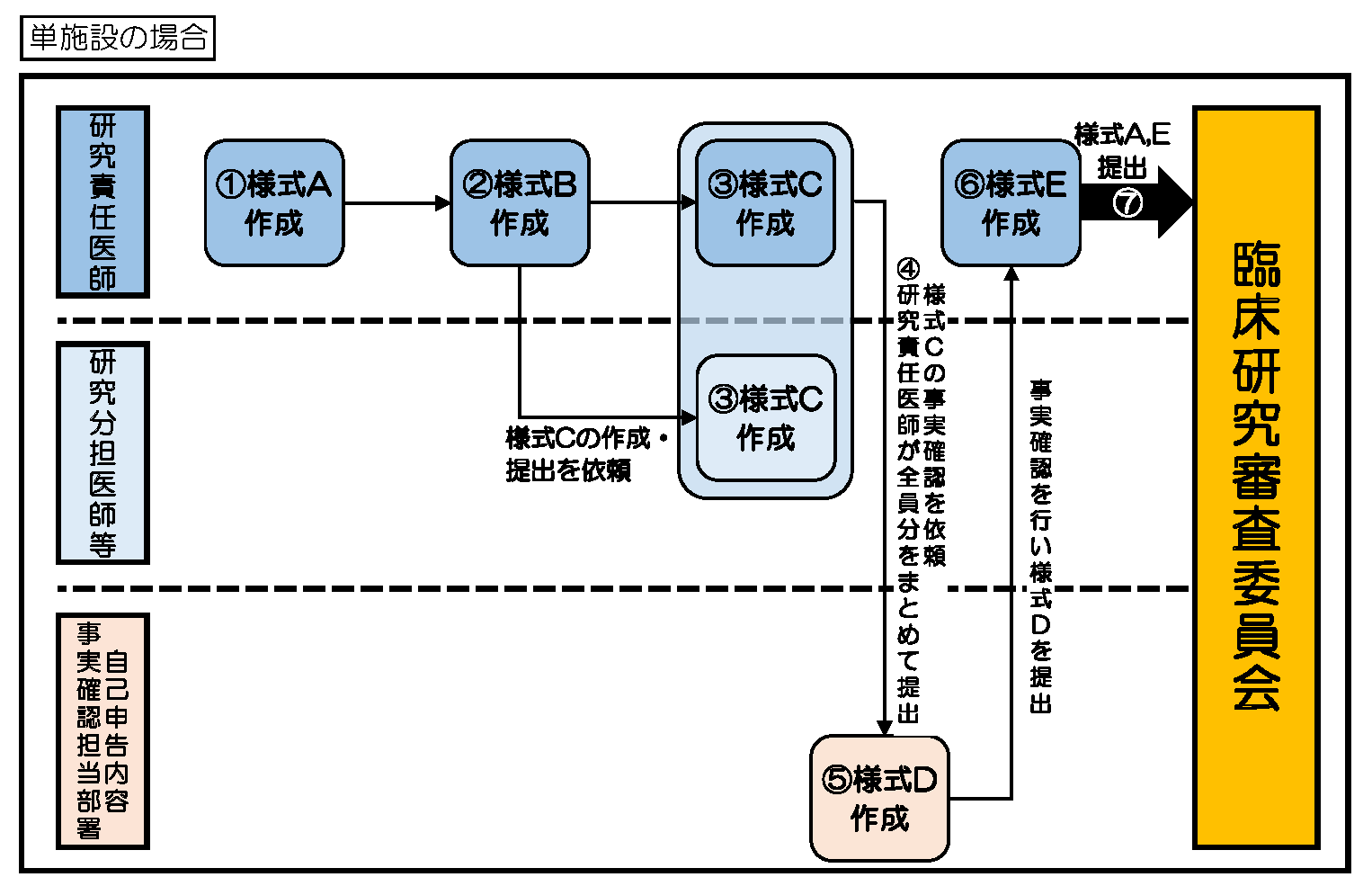
① 様式Aを作成。(研究責任医師)
② 様式Bを作成。(研究責任医師)
③ 様式Cを作成。(研究責任医師、研究分担医師)
④ 研究責任医師、研究分担医師全員分の様式Cをとりまとめ、所属機関の担当部署に提出し、様式Cの内容の事実確認を依頼。(研究責任医師)
⑤ 様式Cの内容の事実確認を行い、様式Dを作成、研究責任医師へ返送。(所属機関の事実確認担当部署)
⑥ ⑤で返送された様式Dを基に、様式Eを作成。(研究責任医師)
⑦ 様式Aと様式Eを他の申請書類とともにCRB審査申請システムにてCRB事務局へ提出。(研究責任医師)
※ 大阪公立大学医学部附属病院の研究責任医師は、①~⑥を利益相反Web申告システム内で行う。
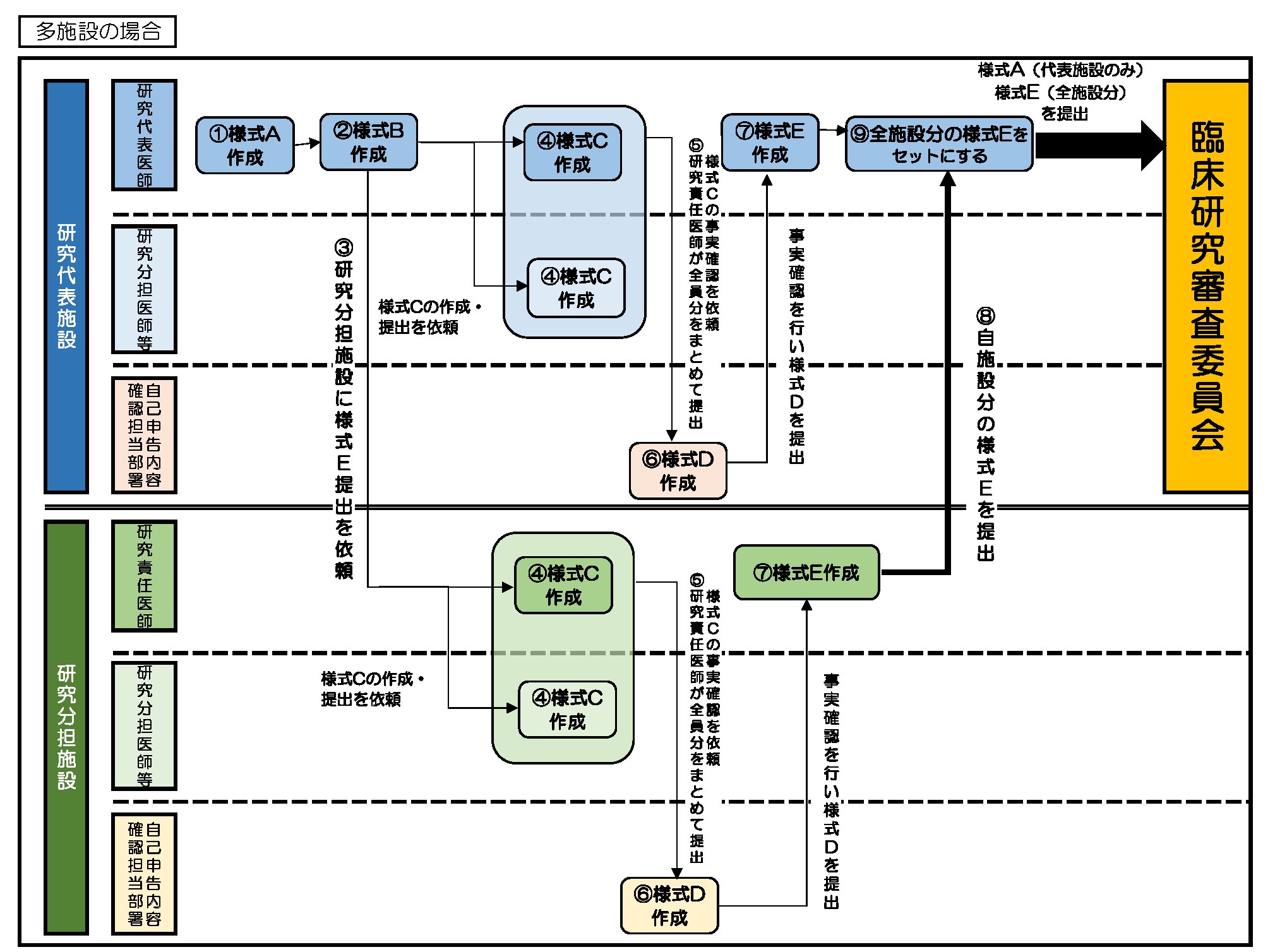
・研究代表施設の揚合
① 様式Aを作成。(研究代表医師)
② 様式Bを作成。(研究代表医師)
③ 研究分担施設の研究責任医師へ様式Aと様式Bを送付し、様式Eの提出を依頼する。(研究代表医師)
④ 自施設の様式Cを作成。(研究代表医師、研究分担医師)
⑤ 自施設の研究代表医師、研究分担医師全員分の様式Cをとりまとめ、所属機関の事実確認担当部署に提出し、様式Cの内容の事実確認を依頼。(研究代表医師)
⑥ 様式Cの内容の事実確認を行い、様式Dを作成、研究代表医師へ返送。(所属機関の事実確認担当部署)
⑦ ⑥で返送された様式Dを基に、様式Eを作成。(研究代表医師)
⑧ 研究代表医師へ自施設の様式Eを提出。(研究分担施設の研究責任医師)
⑨ 自施設と研究分担施設全施設分の様式Eを取りまとめ、様式Aと様式Eを他の申請書類とともにCRB審査申請システムにてCRB事務局へ提出。(研究代表医師)
※ 大阪公立大学医学部附属病院の研究代表医師は、①②④~⑦を利益相反web申告システム内で行う。
・研究分担施設の揚合
① 研究代表施設で様式Aを作成。(研究代表医師)
② 研究代表施設で様式Bを作成。(研究代表医師)
③ 研究分担施設の研究責任医師へ様式Aと様式Bを送付し、様式Eの提出を依頼する。(研究代表医師)
④ 自施設の様式Cを作成。(研究責任医師、研究分担医師)
⑤ 自施設の研究責任医師、研究分担医師全員分の様式Cをとりまとめ、所属機関の事実確認担当部署に提出し、様式Cの内容の事実確認を依頼。(研究責任医師)
⑥ 様式Cの内容の事実確認を行い、様式Dを作成、研究責任医師へ返送。(所属機関の事実確認担当部署)
⑦ ⑥で返送された様式Dを基に、様式Eを作成。(研究責任医師)
⑧ 研究代表医師へ自施設の様式Eを提出。(研究責任医師)
※ 大阪公立大学医学部附属病院の研究責任医師は、④~⑦を利益相反web申告システム内で行う。