各種報告・届出
研究開始から研究終了後について
臨床研究法に基づき策定し、公表された実施計画を元に、実施基準を遵守して研究を実施する必要があります。
研究実施中に遵守すべき事項
・臨床研究法、研究計画書の遵守・インフォームド・コンセントの取得
・医薬品等の品質確保
・健康被害の補償、医療の提供
・記録の作成、保存
・秘密保持
・各種申請手続き(変更申請、疾病等報告、定期報告、不適合報告)
・利益相反管理
・jRCTの登録情報の更新
・実施計画変更の届出(特定臨床研究のみ)
・モニタリング
・監査(必要に応じて)
研究終了後に遵守すべき事項
・認定臨床研究審査委員会及び実施医療機関の管理者へ主要評価項目報告書、総括報告書、総括報告書の概要の提出・厚生労働省へ総括報告書の概要の提出
・jRCTへ総括報告書の概要の登録
・認定臨床研究審査委員会及び実施医療機関の管理者への研究終了報告
・記録の保管
実施計画の提出
実施計画を厚生労働大臣へ提出し、jRCTへの公表を行った場合は、実施医療機関の管理者へ報告する必要があります。・実施計画提出報告書 (大阪公立大学様式)
定期報告
統括管理者は、臨床研究の実施状況・疾病等の発生状況について、実施計画を厚生労働大臣に提出した日(jRCTで公表された日)から1年毎に報告しなければならないと定められています。
実施医療機関の管理者に報告したうえで、認定臨床研究審査委員会へ報告し、認定臨床研究審査委員会が意見を述べた日から起算して1ヵ月以内に厚生労働大臣への報告を行なうことが義務付けられています。
実施医療機関の管理者及び認定臨床研究審査委員会への定期報告
【報告事項】
・臨床研究に参加した対象者の数
・臨床研究に係る疾病等の発生状況及びその後の経過
・省令又は研究計画書に対する不適合の発生状況及びその後の対応
・安全性及び科学的妥当性についての評価
・管理が必要な利益相反の関与に関する事項
【報告時期】
実施計画を厚生労働大臣に提出した日から起算して1年ごとに、当該期間満了後2ヵ月以内
【報告様式】
・定期報告書(統一書式5)
厚生労働大臣への定期報告
【報告事項】
・実施計画に記載されている認定臨床研究審査委員会の名称
・当該委員会による研究継続の適否
・臨床研究に参加した対象者の数
【報告時期】
認定臨床研究審査委員会が意見を述べた日から起算して1ヵ月以内
【報告様式】
・定期報告書(別紙様式3) 記載例
※jRCTで必要事項を入力し、一時保存したものを出力してご提出ください。
疾病報告・不具合報告
研究責任医師は、臨床研究の実施中に研究の実施によると疑われる疾病等が発生した場合は、厚生労働大臣並びに認定臨床研究審査委員会へ報告することが義務付けられています。
疾病等の区分により、7日、15日、30日等の報告期限が定められています。
参考資料:厚生労働省 第13回厚生科学審議会臨床研究部会
「09参考資料1_部会参考資料1 疾病等報告の部会での報告」
研究実施中に下記の事項が発生したことを知った研究責任医師は、各々に定める期間内に認定臨床研究審査委員会へ報告することが義務付けられています。
報告の対象となるのは、特定臨床研究の実施によると疑われる疾病・不具合です。
厚生労働大臣への報告は、jRCT(臨床研究実施計画・研究概要公開システム)の疾病等報告より行ってください。
医薬品を用いる特定臨床研究
| PMDA | 委員会 | 定期報告 | ||||
|---|---|---|---|---|---|---|
| 未承認・適応外 | 医薬品等 | 未知 | 死亡 | 7日 | 7日 | ○ |
| 重篤 | 15日 | 15日 | ○ | |||
| 非重篤 | 定期 | ○ | ||||
| 既知 | 死亡 | 15日 | ○ | |||
| 重篤 | 定期 | ○ | ||||
| 非重篤 | 定期 | ○ | ||||
| 不具合 (医療機器、再生医療等製品) |
未知 | 死亡のおそれ | 30日 | |||
| 重篤のおそれ | 30日 | |||||
| 非重篤のおそれ | ||||||
| 既知 | 死亡のおそれ | 30日 | ||||
| 重篤のおそれ | 30日 | |||||
| 非重篤のおそれ | ||||||
| 既承認 | 医薬品等 | 未知 | 死亡 | 15日 | ○ | |
| 重篤 | 15日 | ○ | ||||
| 非重篤 | 定期 | ○ | ||||
| 既知 | 死亡 | 15日 | ○ | |||
| 重篤 | 30日 | ○ | ||||
| 非重篤 | 定期 | ○ | ||||
| 感染症 | 未知 | 死亡・重篤 | 15日 | ○ | ||
| 非重篤 | 15日 | ○ | ||||
| 既知 | 死亡・重篤 | 15日 | ○ | |||
| 非重篤 | 定期 | ○ | ||||
| 不具合 (医療機器、再生医療等製品) |
重篤(死亡含む)のおそれ | 30日 | ||||
| 未知 | 非重篤のおそれ | |||||
| 既知 | 非重篤のおそれ | |||||
認定臨床研究審査委員会への報告
【報告様式】
・医薬品疾病等報告書(統一書式8)
・医療機器疾病等又は不具合報告書(統一書式9)
・再生医療等製品疾病等又は不具合報告書(統一書式10)
・詳細記載用書式
厚生労働大臣への報告
厚生労働大臣へ疾病等報告を行なう場合は、jRCT(臨床研究実施計画・研究概要公開システム)より必要事項を入力し、PMDAへ送信してください。
疾病等報告のフロー(単施設)
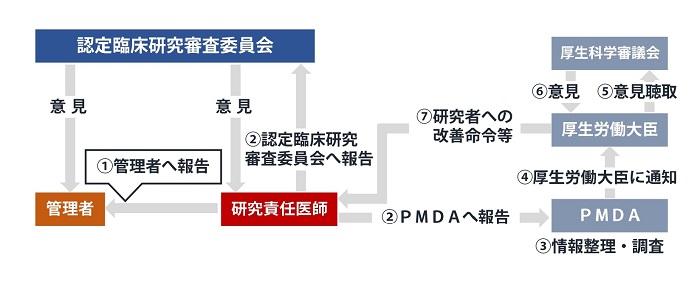

疾病等報告のフロー(多施設共同研究)
事例:参加施設A病院で特定臨床研究による疾病等が発生した場合
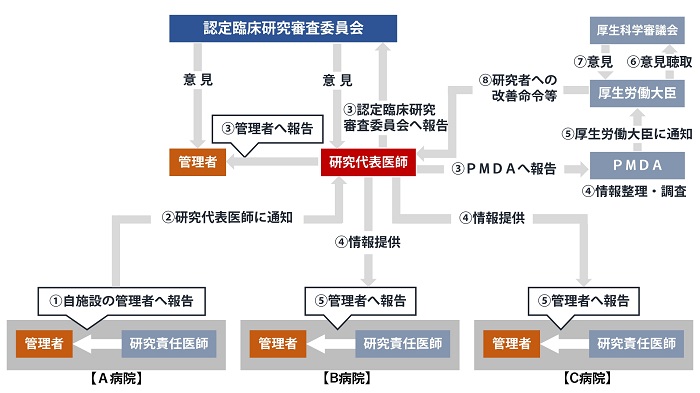
【当院が分担施設として参加している場合の報告様式】
・医薬品疾病等報告書(統一書式8)
・医療機器疾病等又は不具合報告書(統一書式9)
・再生医療等製品疾病等又は不具合報告書(統一書式10)
・詳細記載用書式 ※必要な場合
不適合報告
研究責任医師は、臨床研究が臨床研究法施行規則または研究計画書に不適合(適合していない状態)であると知ったときは実施医療機関の管理者に報告することが義務付けられています。
また不適合のうち、特に重大なものが判明したとき*1は、速やかに認定臨床研究審査委員会へ審議を依頼し、委員会の意見を聴いたうえで1ヵ月以内に実施医療機関の管理者へ報告することが定められています。
*1:臨床研究の対象者の人権や安全性及び研究の進捗や結果の信頼性に影響を及ぼすものをいう。
実施医療機関の管理者及び認定臨床研究審査委員会への報告
【報告様式】
・重大な不適合報告書(統一書式7)
・不適合報告書(当院病院長への報告用)
【多施設共同研究で当院が分担施設である場合の報告様式】
・重大な不適合報告書
・不適合報告書
事務局までご提出ください。

中止報告
特定臨床研究を中止したときは、その中止の日から10日以内に認定臨床研究審査委員会に通知し、厚生労働大臣に届け出なければならないと定められています。
・臨床研究を中止する場合は、当該臨床研究の対象者に適切な措置を講じてください。
・必要に応じて対象者の措置に伴う研究終了時期やその方法について、認定臨床研究審査委員会の意見を聴いてください。
・臨床研究を中止した場合であっても、臨床研究終了(例えば、がん臨床研究においては、中止前の最終登録症例がフォローアップ期間終了になるまでは臨床研究期間となる)までは、疾病等報告、定期報告を行ってください。
・研究計画に変更が生じた場合には、変更事項の届出を行ってください。
・臨床研究を中止した場合であっても、中止した日または全ての評価項目に係るデータの収集を行うための期間が終了した日のいずれか遅い日から原則一年以内に総括報告書を提出しなければなりません。
認定臨床研究審査委員会への通知
【通知様式】
・中止通知書(統一書式11)
事務局までご提出ください。
厚生労働大臣への届出
【届出様式】
・特定臨床研究中止届書(様式第4)
※jRCTで必要事項を入力し、一時保存したものを出力してご提出ください。
終了報告
統括管理者は、以下を作成し、認定臨床研究審査委員会の意見を聴いたうえで厚生労働大臣へ報告することが定められています。
・主要評価項目報告書
主要評価項目データの収集期間が終了した日から1年以内
・総括報告書・総括報告書の概要(総括報告書の概要は終了届書(別紙様式1)で差し支えない)
全てのデータの収集期間が終了した日から1年以内
認定臨床研究審査委員会への通知
【通知様式】
・終了通知書(統一書式12)
事務局までご提出ください。
厚生労働大臣への届出
【届出様式】
・終了届書(別紙様式1)
※jRCTで必要事項を入力し、一時保存したものを出力してご提出ください。
