最新の研究成果
副作用の少ない抗がん剤の開発を目指して ~輸送タンパク質L-PGDSを用いたDDSで、がん組織だけに送達~
2026年3月5日
- 農学研究科
- プレスリリース
発表者
大阪公立大学大学院農学研究科 乾 隆教授、古田 航祐氏(研究当時、大学院生)、
中辻 匡俊博士(研究当時、大学院生)、山村 堯樹客員研究員
概要
近年開発されている薬剤は、低分子化合物の中でも分子量※1が比較的大きく、難水溶性のため、体内に吸収されにくいという課題があります。そのため、抗がん剤などを効果的に溶かし、がん組織だけに効率よく届けるドラッグデリバリーシステム(DDS)の開発が活発に行われています。本研究グループは、生体内輸送タンパク質であるリポカリン型プロスタグランジンD合成酵素(L-PGDS)※2を利用し、分子量が大きく、難水溶性の抗がん剤Paclitaxel(パクリタキセル、以降PTX)を効果的に溶かし、がん細胞に効率的に運搬できるDDSキャリアを開発しました。
本研究成果は、2025年12月31日に化学や材料工学などを対象とする国際学術誌「ACS omega」にオンライン掲載されました。
ポイント
- 生体内輸送タンパク質L‑PGDSをDDSキャリアとして活用し、分子量が比較的大きい難水溶性の抗がん剤PTXを効率よく輸送する手法を開発。
- L‑PGDSにPTXを結合させると溶解度が約3,600倍向上した。さらに、L‑PGDSに標的化ペプチドCRGDKを付加すると、がん組織を標的に送達することが可能になり、高い抗腫瘍効果が示された。
- 乳がん細胞を移植したマウスモデルを用いて抗腫瘍効果を評価したところ、PTX/L-PGDSおよびPTX/L-PGDS-CRGDKは投与終了後も抗腫瘍効果を維持し、特にPTX/L-PGDS-CRGDKは最も高い腫瘍抑制効果を示した。
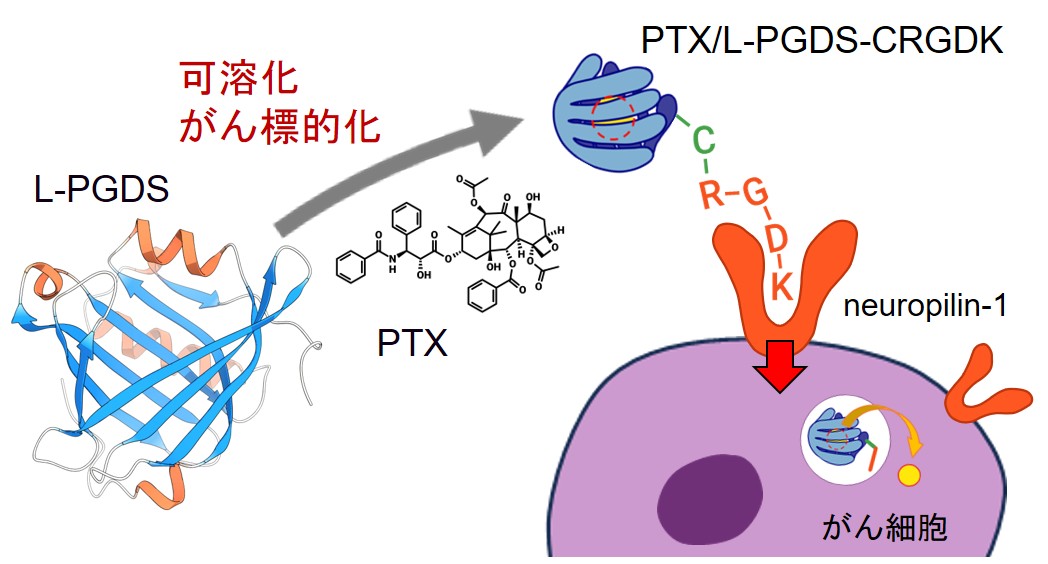 図1:L-PGDS-CRGDKによるPTXに対するがん標的化DDS
図1:L-PGDS-CRGDKによるPTXに対するがん標的化DDS
<研究者のコメント>
強い副作用で治療継続が難しい進行がん患者さんを一人でも救いたい、という思いで研究を続けています。L-PGDSを利用した新しい抗がん剤内包DDS製剤で、安全性と有効性を両立し、化学療法の限界突破を目指します。
研究の背景
近年、創薬研究の進展により、高い薬効を有する医薬候補化合物が数多く開発されています。しかし、このような候補化合物の多くは、分子量が大きく、水に溶けにくいなどの性質を持つことから、取り扱いが難しく、また生体内への吸収が乏しいため十分な治療効果を発揮させることが困難であることが課題となっています。さらに、抗がん剤の場合、水に溶けにくいことに加えて、薬剤が正常組織にも分布してしまうことで強い副作用が生じることが大きな問題となっています。高い薬効を有するにも関わらず、難水溶性のために開発が困難な抗がん剤、あるいはその候補化合物を効果的に可溶化し、且つがん組織へ効率よく届けるドラッグデリバリーシステム(drug delivery system, DDS)の開発が活発に行われています。本研究グループは、哺乳動物の中枢神経系に高発現し、さまざまな疎水性低分子を結合する生体内輸送タンパク質であるリポカリン型プロスタグランジンD合成酵素(L-PGDS)に着目し、難水溶性薬剤を可溶化し、疾患部位へ輸送するDDSの開発を進めてきました。
研究の内容
本研究では、分子量が比較的大きく、難水溶性の抗がん剤であるPaclitaxel(PTX、分子量 854)を効率的に運搬する新たなDDSキャリアとしてL-PGDSを利用し、さらにがん組織特異的に輸送するDDSの開発を試みました(図1)。
ドッキングシミュレーションおよび溶解試験により、PTXはL-PGDSのβバレル上部に主に疎水性相互作用を介して結合し、またその溶解度をリン酸緩衝液中と比較して、約3,600倍改善することを明らかにしました。さらに、がん組織への選択的送達を目的として、がん細胞表面に発現するneuropilin-1という受容体に結合する標的化ペプチドCRGDKを、L-PGDSのC末端に結合させたL-PGDS-CRGDKを作製しました。そこで、MDA-MB-231乳がん細胞を移植したマウスモデルを用いて抗腫瘍効果を評価したところ、市販製剤であるタキソールは投与期間中に抗腫瘍効果を示したものの、投与終了後には効果が減弱しました。これに対し、PTX/L-PGDSおよびPTX/L-PGDS-CRGDKは投与終了後も抗腫瘍効果を維持し、特にPTX/L-PGDS-CRGDKは最も高い腫瘍抑制効果を示しました。
これらの結果から、L-PGDSにがん標的化ペプチドを付加したL-PGDS-CRGDKは、854という大きい分子量を有する難水溶性抗がん剤のPTXを内包し、且つがん細胞特異的に標的化できる有望なDDSキャリアであることが示唆されました。
期待される効果・今後の展開
本研究により、L-PGDSが分子量約850までの比較的大きな薬剤も結合でき、さらに標的化ペプチドを導入することで、がん細胞選択的に抗がん剤を輸送できることを明らかにしました。本DDSは、難溶性抗がん剤の新たな送達戦略として、今後のがん治療の高度化に大いに貢献することが期待されます。
資金情報
本研究の一部は、日本学術振興会(JSPS)科研費 基盤研究A(25242046)からの支援を受けて実施しました。
用語解説
※1 分子量:典型的な低分子化合物の分子量は約300〜500 である。低分子化合物の中でも比較的高分子量とされる領域は、約600〜1000 を指すことが多い。
※2 リポカリン型プロスタグランジンD合成酵素(L-PGDS):プロスタグランジンD2を合成する酵素であるが、同時に脂溶性の低分子を運ぶ 「運び屋タンパク質(キャリア)」 としても働く。βバレル構造をもつリポカリンファミリーの分泌タンパク質であり、ヒトの脳脊髄液中に多く存在し、脂溶性物質を疎水性ポケットに取り込んで運べるため、難水溶性薬物のDDSキャリアとして注目されている。
掲載誌情報
【発表雑誌】 ACS omega
【論文名】 Drug Delivery System for the Anticancer Drug Paclitaxel Using Lipocalin-Type Prostaglandin D Synthase Conjugated to a Tumor-Targeting Peptide
【著者】 古田 航祐、中辻 匡俊、吉田 はるな、大久保 理奈、西出 圭佑、山村 堯樹、乾 隆
【掲載URL】 https://doi.org/10.1021/acsomega.5c09324
研究内容に関する問い合わせ先
大阪公立大学大学院農学研究科
教授 乾 隆(いぬい たかし)
TEL:072-254-9473
E-mail:inuit[at]omu.ac.jp
※[at]を@に変更してください。
報道に関する問い合わせ先
大阪公立大学 広報課
担当:谷
TEL:06-6967-1834
E-mail:koho-list[at]ml.omu.ac.jp
※[at]を@に変更してください。
該当するSDGs

